Cos'è OVR nella chimica moderna?
Parliamo di cosa è OVR nella sintesi inorganica e organica.
Definizione del processo
Sotto reazioni redox coinvolgono processi quali la conseguenza che cambierà lo stato di ossidazione di due o più elementi chimici di sostanze complesse o semplici.

Cos'è l'ossidazione?
Per ossidazione si intende una sostanza chimicauna reazione in cui un atomo o uno ione specifico emette elettroni, mentre diminuisce il suo stato iniziale di ossidazione. Questo processo è tipico per i metalli.
Cos'è il recupero?
Con il processo di restauro si intendetrasformazione chimica, che si tradurrà in una diminuzione del grado di ossidazione nello ione o di una sostanza semplice, con l'aggiunta di elettroni. Questa reazione è caratteristica per non metalli e residui acidi.

Caratteristiche dell'agente riducente
Considerando la domanda su cosa sia OVR, non si può ignorare una tale idea di "riduttante".
Con esso si intende una molecola neutra oione caricato, che a seguito dell'interazione chimica darà l'altro ione o atomo di elettrone, aumentando il suo grado di ossidazione.
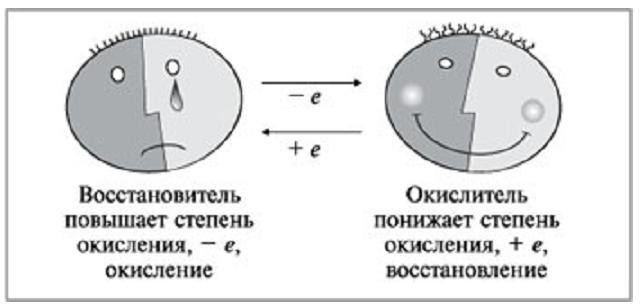
Determinazione dell'ossidante
Discutere su ciò che è OVR è anche importantemenziona anche un termine come "ossidante". Con ciò, è consuetudine significare tali ioni o atomi neutri che, durante l'interazione chimica, prenderanno elettroni negativi da altri atomi o particelle neutre. Allo stesso tempo, il suo stato di ossidazione iniziale diminuirà.
Tipi di OBR
Discutendo su ciò che è OVR, è necessario prendere nota di quelle varietà di questi processi, che sono spesso considerati nella sintesi inorganica e organica.
Le interazioni molecolari assumono taleprocessi in cui gli atomi di entrambi l'agente riducente e l'ossidante si trovano in diversi materiali di partenza che entrano in interazione. Un esempio di questo tipo di trasformazione è l'interazione tra l'ossido di manganese (4) e l'acido cloridrico, che si traduce in cloro gassoso, cloruro di manganese bivalente e acqua.
In questo processo chimico, comegli anioni del cloro appaiono ossidanti mentre interagiscono. Il catione di manganese (con stato di ossidazione +4) mostra capacità ossidative nella reazione, prendendo due elettroni, viene ripristinato.
L'interazione intramolecolare ètali trasformazioni chimiche, nella misura in cui sia gli atomi dell'agente riducente che gli atomi dell'ossidatore sono inizialmente una sostanza fonte, e dopo il completamento della trasformazione si trovano in vari prodotti di reazione.
Come esempio di questo tipo di reazione,rappresentare la decomposizione del clorato di potassio. Una volta riscaldata, questa sostanza si trasformerà in cloruro di potassio e ossigeno. Le proprietà ossidanti saranno caratteristiche per l'anione clorato, che, prendendo cinque elettroni nella reazione, sarà ridotto al cloruro.
In questo caso, l'anione dell'ossigeno si manifesteràproprietà riducenti, ossidanti a ossigeno molecolare. Quindi cos'è OVR in questo caso? Questo è il processo di trasferimento di elettroni tra gli ioni, che porta alla formazione di due prodotti di reazione.
Anche a questo tipo di trasformazione chimica,verificarsi con un cambiamento nei gradi di ossidazione di elementi originariamente trovati in una formula, è il processo di decomposizione del nitrito di ammonio. L'azoto, che si trova nel catione di ammonio, ha un grado di ossidazione -3, durante il processo cede sei elettroni e viene ossidato in azoto molecolare. E quell'azoto, che fa parte del nitrito, prende sei elettroni, mentre è un agente riducente e durante la reazione è ossidato.
Cos'è OVR in chimica? La definizione sopra considerata mostra che si tratta di trasformazioni associate a cambiamenti in diversi elementi degli stati di ossidazione.
Autoossidazione e riduzione (sproporzione)assume tali processi, nel corso dei quali, come agente riducente e un ossidante, c'è un atomo iniziale che aumenterà e contemporaneamente ridurrà il suo stato di ossidazione dopo il completamento dell'interazione. Discutendo su ciò che è OVR in chimica, esempi di tali trasformazioni possono essere trovati anche nel corso di chimica nella scuola secondaria. La decomposizione del solfito di potassio al riscaldamento porta alla formazione di due sali di questo metallo: solfuro e solfato. Lo zolfo con uno stato di ossidazione di +4 mostra sia proprietà riducenti che ossidanti, aumentando e diminuendo lo stato di ossidazione.

Per capire cosa significa OVI in chimica, chiamiamoloun altro tipo di tali trasformazioni chimiche. La controproporzione implica tali processi, in conseguenza dei quali gli atomi dell'agente riducente e dell'ossidatore si trovano nella composizione di diversi componenti iniziali, ma sul lato destro formano un prodotto di reazione. Ad esempio, nell'interazione dell'ossido di zolfo (4) con idrogeno solforato si formeranno zolfo e acqua. Uno ione di zolfo con uno stato di ossidazione di +4 impiegherà quattro elettroni e uno ione di zolfo con un esponente -2 perderà due elettroni. Di conseguenza, entrambi si trasformano in una sostanza semplice, in cui il grado di ossidazione è zero.

conclusione
Considerando la domanda su cosa sia OVR in chimica,notiamo che si tratta di numerose trasformazioni, attraverso le quali funzionano gli organismi viventi, si verificano vari processi e fenomeni naturali. Al fine di disporre i coefficienti in tali equazioni, è necessario compilare un bilancio elettronico.






